PCTI 251-SC-Expresión de Taq polimerasa recombinante en E.coli TOP10 para su producción a bajo costo
Carlos Angulo
Autor de Correspondencia
Dr. Héctor Nolasco Soria
Editor
24/11/2025
Fecha de Aprobación
Biotecnología y Ciencias Agropecuarias
Categoría
Autores
Alberto Pedrína, Hassian León-Montoyab, Reyna de Jesús Romero-Geraldoa, Carlos Angulob
aTecnológico Nacional de México-Instituto Tecnológico de La Paz. La Paz, B.C.S
bCentro de Investigaciones Biológicas del Noroeste, S.C. (CIBNOR). Grupo de Inmunología y Vacunología, La Paz, B.C.S. eangulo@cibnor.mx.
La enzima polimerasa tiene como función principal generar nuevas copias de una cadena de ADN. Las condiciones de crecimiento de T. aquaticus dificultan la producción de Taq polimerasa y elevan el precio de venta, por esta razón se buscan alternativas para la producción de esta enzima.
Glosario de términos técnicos:
Enzima: proteína capaz de acelerar una reacción química en los organismos vivos, actuando como un catalizador (Tortora et al., 2019).
ADN (Ácido desoxirribonucleico): molécula bicatenaria que almacena la información genética de los organismos y dirige la producción de proteínas (Watson & Krieg., 1953; Martínez-Frías et al., 2010).
PCR (Reacción en cadena de la polimerasa): técnica utilizada en biología molecular que replica secuencias específicas de ADN mediante ciclos repetidos de desnaturalización, alineamiento y extensión (Mullis, 1990).
Electroforesis SDS-PAGE: método que separa proteínas según su peso molecular usando un gel de poliacrilamida y SDS para desnaturalizarlas y otorgarles carga idéntica (Laemmli, 1970).
pTTQ18: ADN circular o plásmido de expresión bacteriano que contiene un promotor fuerte (tac), un gen que brinda resistencia a antibióticos y un origen de replicación para generar más copias. Este pTTQ18 usado para producir proteínas recombinantes en E. coli (Gómez et al., 2002).
Abstract
The main function of the polymerase enzyme is to generate new copies of a DNA strand. An example of this enzyme is Taq polymerase, known for its thermal stability. However, Taq polymerase is commercially expensive; therefore, alternatives are sought for simple, functional, and low-cost production. This work aims to express functional Taq polymerase for application in the polymerase chain reaction. From a transformed and cultured colony of Escherichia coli TOP10 strain, the expression of the enzyme was induced with isopropyl β-D-1-thiogalactopyranoside (IPTG), followed by an incubation at 37 °C for 72 hours. Later, the enzyme was extracted by using buffer A and buffer B and stored at 4 °C in a storage buffer. Then, the enzyme protein integrity was evaluated by SDS-PAGE electrophoresis. Thereafter, an endpoint PCR was performed using 1 and 2 μL of the protein extract. Finally, the concentration of Taq polymerase in the protein extract was determined using the ImageJ software. The presence of Taq polymerase was identified at 94 kDa with a concentration between 135-196 ng/μL. The best PCR amplification was with 1 μL of extract compared to 2 μL of the extract. In conclusion, E. coli produced the enzyme Taq polymerase functionally for application in PCR.
Keywords: bioproduction, protein, molecular biology, genetic engineering
Resumen:
La enzima polimerasa tiene como función principal generar nuevas copias de una cadena de ADN; ejemplo de esta enzima es la Taq polimerasa, la cual destaca por su estabilidad térmica. Sin embargo, la Taq polimerasa tiene un alto costo comercial; por lo tanto, se buscan alternativas para una producción sencilla y a bajo costo. Este trabajo tiene como objetivo expresar Taq polimerasa funcional para su aplicación dentro de PCR. La expresión de la enzima Taq polimerasa se indujo con isopropil β-D-1-tiogalactopiranósido (IPTG) en cepas Escherichia coli TOP10 a 37 °C por 72 horas. Después, la extracción de la enzima se realizó mediante los buffers A y B, un baño María y se guardó con buffer de almacenamiento a 4 °C. La integridad de la enzima se evaluó mediante electroforesis SDS PAGE y una PCR de punto final con 1 y 2 μL del extracto proteico; finalmente, la concentración de la Taq polimerasa en el extracto proteico se determinó mediante densitometría con el software ImageJ. La presencia de Taq polimerasa se identificó como una banda de 94 kDa, y una concentración entre 135-196 ng/μL del extracto. La mejor amplificación por PCR fue con 1 μLde extracto en comparación con 2 μL. En conclusión, E. coli produjo la enzima Taq polimerasa de forma funcional para su aplicación en la PCR.
Palabras Clave: Bioproducción, proteína, biología molecular, ingeniería genética
Problemática
Usuarios
Proyecto
Introducción:
En las células existen las enzimas llamadas ADN polimerasas, las cuales tiene la función de generar nuevas copias de las cadenas de material genético (Tortora et al., 2019). Esta cualidad es aprovechada en los laboratorios para aplicarse en la identificación parental, enfermedades genéticas, patógenos; entre otras, mediante la técnica de reacción en cadena de la polimerasa (PCR). Las bacterias también cuentan con ADN polimerasas, pero específicamente la bacteria Thermus aquaticus produce una ADN polimerasa llamada “Taq polimerasa” descubierta en los años 70’s (Chien et al., 1976). La enzima Taq polimerasa destaca por su estabilidad térmica a temperaturas de 80-95 °C, y por ello es utilizada en técnicas de biología molecular como la PCR (Ishino & Ishino, 2014). Sin embargo, las condiciones de crecimiento de T. aquaticus dificultan la producción de Taq polimerasa y elevan el precio de venta (Chien et al., 1976). Por esta razón se buscan alternativas para la producción de esta enzima.
Las alternativas que se han llevado a cabo para reducir costos son su producción en levadura (Saccharomyces cerevisiae) o bacterias como Vibrio natriegens y Escherichia coli (Hriňová et al., 2024; Zhra et al., 2024). Particularmente, en E. coli se ha realizado la producción en sistemas de expresión pET y métodos de purificación basados en la afinidad a metales, lo que añade costos de procesamiento (Abeldenov & Khassenov, 2014). Una alternativa más barata es el uso directo de extractos de E. coli productora de Taq polimerasa en PCR (Lee et al., 2023). Las cepas de E. coli JM109, DH5α y BL21 son ampliamente utilizadas para la producción de Taq. Mientras que cepas como E. coli TOP10, comúnmente utilizada para clonación de vectores, ha sido poco explorada como producción enzimática (Gómez et al., 2002; Ferralli et al., 2007; Abeldenov et al., 2014; Hriňová et al., 2024).
Para la producción de esta enzima en E. coli se utiliza un vehículo genético llamado pTTQ18 (Figura 1), el cual contiene el gen Taq polimerasa (Gómez et al., 2002). Los componentes de este vehículo genético, nos permiten controlar el momento del inicio de la producción de Taq polimerasa dentro de E. coli mediante el uso de una molécula activadora (inductor). Además, la extracción, almacenamiento y estabilidad de la enzima puede mejorarse mediante la utilización de soluciones específicas compuestas de Tris-HCl, dextrosa, EDTA, DTT, detergentes y/o glicerol (Ferralli et al., 2007). Este enfoque ofrece una alternativa accesible y reproducible, particularmente en laboratorios con recursos limitados, y permite generar cantidades suficientes de enzima para su uso en PCR, demostrando tanto su viabilidad práctica como su potencial aplicación educativa y de transferencia tecnológica.
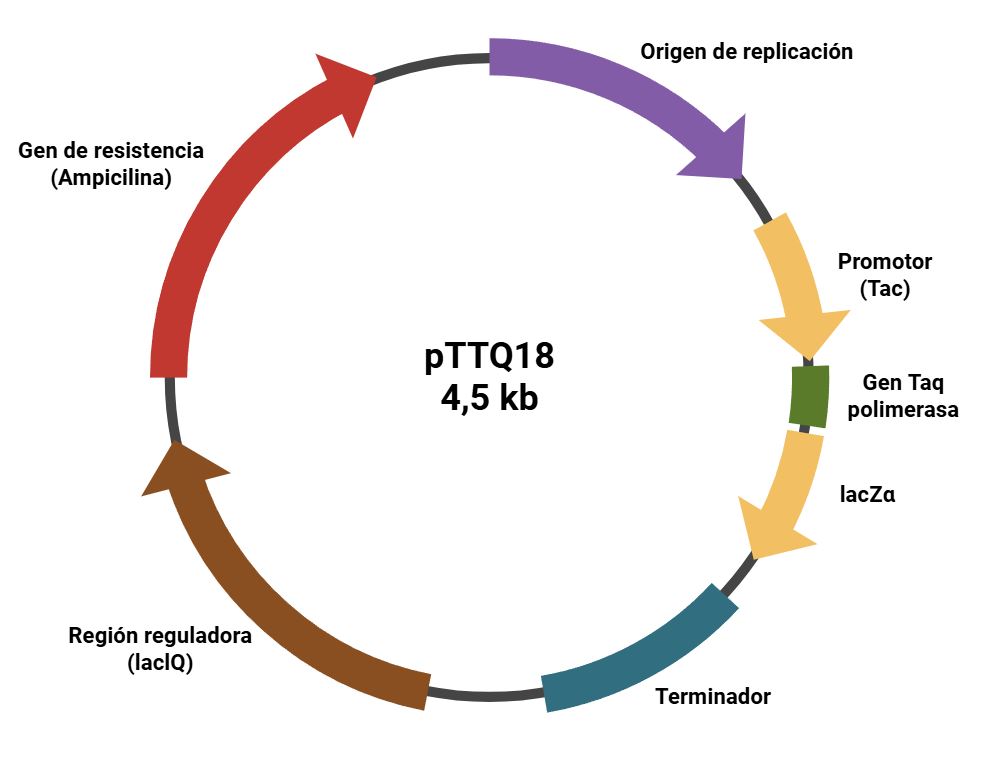
Figura 1. Vector pTTQ18, utilizado en E. coli TOP10 para expresar Taq polimerasa.
Objetivo: Expresar Taq polimerasa recombinante funcional para su aplicación en PCR.
Materiales y métodos:
Cuatro cultivos independientes de E. coli TOP10 con el plásmido pTTQ18 conteniendo el gen de la Taq polimerasa se sembraron en medio de cultivo LB (10 g/L triptona, 5 g/L extracto de levadura, 10 g/L NaCl, 1.5% agar bacteriológico) con ampicilina (50 mg/L), pH 7.0 ± 0.2. Los cuatro cultivos se incubaron a 37 °C durante 24 horas. Posteriormente, una colonia de E. coli TOP 10 se tomó por picadura y se colocó en 15 mL de caldo LB (10 g/L triptona, 5 g/L extracto de levadura, 10 g/L NaCl) con ampicilina (50 mg/L), pH 7.0 ± 0.2. De cada cultivo se realizó una resiembra y los 4 cultivos resembrados en caldo se incubaron a 37 °C por 72 horas.
Del cultivo E. coli TOP 10 se tomaron 200 μL, la absorbancia de cada muestra se midió a 600 nm y el UFC se determinó mediante una curva de calibración abs vs UFC. Finalmente, en 3 cultivos se agregó 30 μL de isopropil β-D-1-tiogalactopiranósido (0.1 M) y 1 cultivo se apartó como control negativo (sin IPTG). Los 4 cultivos se incubaron a 37 °C por 24 horas.
Después de la incubación, los cultivos se repartieron en microtubos con 1 mL y fueron centrifugados a 8871 x g por 5 min. El sobrenadante de los tubos se decantó y el pellet se resuspendió en 70 μL buffer A (50 mM Tris-HCl pH 7.9,50 mM dextrosa, 1 mM EDTA); el pellet resuspendido se incubó a temperatura ambiente por 10 minutos.
En cada tubo se añadió 70 μL de buffer B (10 mM Tris-HCl pH 7.9, 50 mM KCl, 0.5% Tween 20, 0.5% Triton X-100), los tubos se incubaron en baño María a 75 °C por 30 min y cada 5 minutos se mezcló por inversión. Posteriormente, los tubos se centrifugaron a 9660 x g por 5 minutos y 120 μL se separon en nuevos microtubos. Finalmente, al sobrenadante recuperado se le añadió 120 μL de buffer de almacenamiento (50mM Tris-HCl pH 7.9, 100mM NaCl, 0.5 mM DTT, 1% Triton X-100, 50% Glicerol) y las muestras fueron almacenadas a 4 °C.
La enzima extraída dentro de las muestras se identificó mediante electroforesis SDS-PAGE con 20 μL de extracto, comparando las bandas observadas con un marcador de peso molecular (Precision Plus Protein BIO-RAD). Asimismo, con la Taq polimerasa extraída se realizó una PCR de punto final para evaluar la funcionalidad con 1 μL y 2 μL del extracto proteico (Figura 2). Finalmente, la concentración del extracto proteico a 94 kDa se determinó mediante densitometría con el software ImageJ (https://imagej.net/ij/).
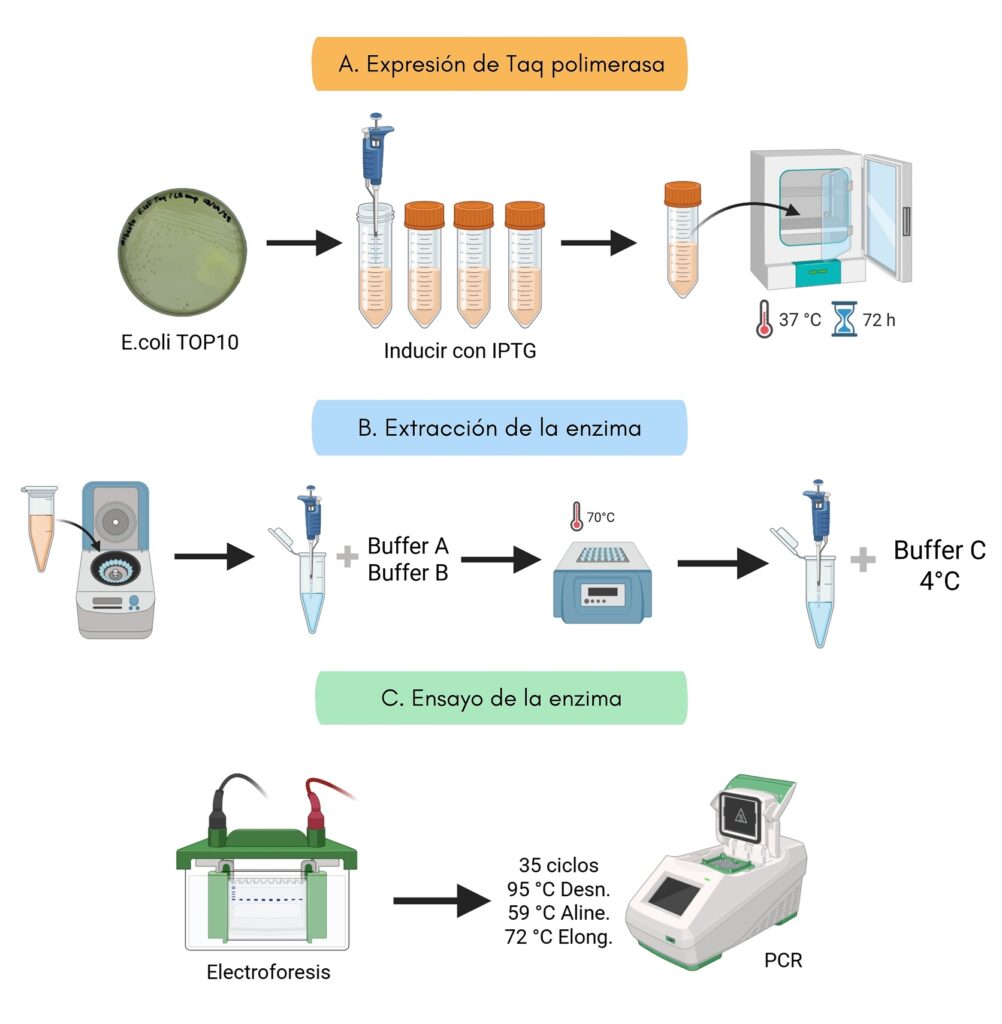
Figura 2. Metodología para la producción de Taq polimerasa recombinante. Paso 1: Cultivar E. coli TOP 10 en medio LB ampicilina. Paso 2: Inducir expresión con IPTG. Paso 3: Incubar a 37°C por 72 horas. Paso 4: Centrifugar y recuperar el pellet. Paso 5: Agregar misma cantidad de buffer A y B. Paso 6: Baño maria por 30 min a 70°C. Paso 7: Agregar misma cantidad de buffer al sobrenadante recuperado. Paso 8: Realizar una electroforesis SDS PAGE. Paso 9: Evaluar enzima en PCR.
Resultados y discusión:
La Taq polimerasa recombinante se identificó a 94 kDa en la electroforesis SDS-PAGE realizada (Figura 3) que corresponde al tamaño esperado de esta enzima (Ferralli et al., 2007). Sin embargo, se puede observar presencia de otras proteínas y es común debido a la presencia de cuerpos de inclusión por proteínas mal plegadas (Bhatwa et al., 2021). Por otro lado, dentro del primer carril se percibe una tenue banda a 94 kDa, que podría corresponder a proteínas endógenas de peso molecular similar a la Taq polimerasa producida (Torres, 2025). Asimismo, comparando con resultados ya publicados, esta tenue banda puede representar una expresión basal del gen de Taq polimerasa cuando no fue realizada una inducción (Fang et al., 2016; Hriňová et al., 2024). Con los extractos se realizó una PCR (Figura 3), y se identificó mayor amplificación con 1 μL en comparación a 2 μL del extracto proteico. Una cantidad alta de enzima como la añadida en 2 μL, en relación con la cantidad de ADN molde y primers, induce efectos negativos como formación de productos no deseados o dímeros de primers (Ingr et al., 2015). Es decir, se pueden desbalancear las concentraciones dentro de la mezcla de componentes de la PCR y así afectar la amplificación del ADN, como lo demostraron Markoulatos et al. (2002). Finalmente, las enzimas presentaron concentraciones de 135-196 ng/μL (Tabla 1) y, en comparación con el control negativo que mostró una expresión basal de la proteína, se observó un ligero incremento en las muestras inducidas con IPTG, tal como lo reportaron Ferralli et al. (2007). Los extractos crudos presentaron concentraciones de 135–196 ng/µL, lo que equivale a aproximadamente 13–39 U/µL, considerando que 1 U corresponde a 5–10 ng de enzima pura. De este modo, la cantidad de proteína obtenida es suficiente para sustituir la dosis estándar de 1 U utilizada en una reacción de PCR de 25 µL, demostrando que la enzima expresada en E. coli TOP10 posee un rendimiento comparable al de las preparaciones comerciales (Promega, 2025). En un análisis comparativo, el costo por reacción de Taq recombinante se estima en 0.37–0.92 MXN, frente a 3.67–9.18 MXN de la Taq comercial, lo que representa hasta 10 veces de ahorro y refuerza su viabilidad económica (ThermoFisher, 2025). Por lo tanto, no solo cepas como E. coli JM109, DH5α y BL21 poseen la capacidad de producir la enzima Taq, sino que también E. coli TOP10 con el vector pTTQ18 puede hacerlo, ofreciendo mayor versatilidad y ampliando las oportunidades de producción con distintas cepas disponibles (Gómez et al., 2002; Ferralli et al., 2007; Abeldenov et al., 2014; Hriňová et al., 2024).
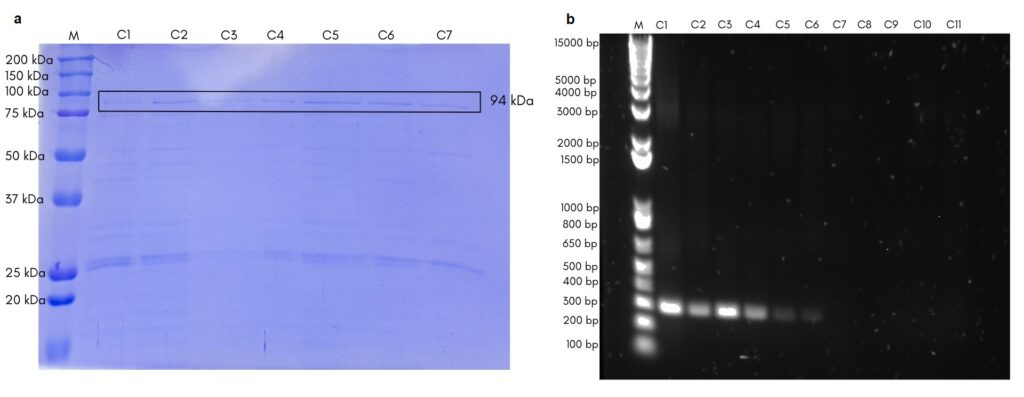
Figura3. (a) Electroforesis SDS PAGE para identificar Taq polimerasa con un tamaño de 94 kDa. Carriles: Marcador (Precision Plus Protein) 1 control negativo (Cultivo no inducido), 2-3 taq recombinante 1, 4-5 taq recombinante 2 y 6-7 taq recombinante 3. (b) Electroforesis de productos de PCR. Carriles: Marcador (1Kb plus) 1 control positivo (taq comercial), 2-4 taq recombinante 1 μL, 5-7 taq recombinante con 2 μL y 9-11 controles negativos.
Conclusiones:
La Taq polimerasa recombinante fue producida en cepas de E. coli TOP 10 que contenían el vector de expresión pTTQ18. Los resultados indican que E. coli TOP 10 produjo la enzima Taq polimerasa con un peso esperado de 94 kDa, con una concentración del extracto proteico entre 135-196 ng/μL y fue funcional en la PCR cuando se utilizó 1 μL de extracto conteniendo la enzima, lo que demuestra su potencial uso en el laboratorio, su aplicabilidad en contextos educativos y de investigación de bajo costo.
Impacto Socioeconómico
La producción de Taq polimerasa recombinante en Escherichia coli es una alternativa para su uso en laboratorio dentro de técnicas como PCR; esta técnica se utiliza de manera cotidiana en la detección de enfermedades genéticas o por patógenos. La producción de esta enzima permite reducir costos por producción de ADN polimerasa a partir de Thermus aquaticus o su obtención de manera comercial.
Referencias
Abeldenov, S. & Khassenov, B. (2014). Cloning, expression and purification of recombinant analog of taq DNA polymerase. https://doi.org/10.11134/btp.1.2014.2
Bhatwa, A., Wang, W., Hassan, Y., Abraham, N., Li, X., & Zhou, T. (2021). Challenges Associated With the Formation of Recombinant Protein Inclusion Bodies in Escherichia coli and Strategies to Address Them for Industrial Applications. In Frontiers in Bioengineering and Biotechnology (Vol. 9). Frontiers Media S.A. https://doi.org/10.3389/fbioe.2021.630551
Chien, A., Edgar, D., & Trela, J. (1976). Deoxyribonucleic acid polymerase from the extreme thermophile Thermus aquaticus. Journal of Bacteriology, 127, 1550–1557. https://doi.org/10.1128/jb.127.3.1550-1557.1976
Fang, N., Zhong, N., Yang, Y., Guo, Y., & Ji, S. (2016). Data of expression and purification of recombinant Taq DNA polymerase. Data in Brief, 9, 81–84. https://doi.org/10.1016/j.dib.2016.08.032
Ferralli, P., Egan, J., & Erickson, F. (2007). Making Taq DNA polymerase in the undergraduate biology laboratory. BIOS, 78, 69–74. https://doi.org/10.1893/0005-3155(2007)78[69:mtdpit]2.0.co;2
Gómez, J., Bermúdez, L., Tamez, R., Adame, J., & de Oca, R. (2002). Producción y purificación de la Taq DNA polimerasa a partir de E. coli recombinante. Ciencia UANL, 5, 316–321.
Hriňová, K., Dlapová, J., Kubala, B., Kormanová, Ľ., Levarski, Z., Struhárňanská, E., Turňa, J., & Stuchlík, S. (2024). Production of Reverse Transcriptase and DNA Polymerase in Bacterial Expression Systems. Bioengineering, 11(7). https://doi.org/10.3390/bioengineering11070727
Ingr, M., Dostál, J., & Majerová, T. (2015). Enzymological description of multitemplate PCR-Shrinking amplification bias by optimizing the polymerase-template ratio. Journal of Theoretical Biology, 382, 178–186. https://doi.org/10.1016/j.jtbi.2015.06.048
Ishino, S., & Ishino, Y. (2014). DNA polymerases as useful reagents for biotechnology – The history of developmental research in the field. In Frontiers in Microbiology (Vol. 5, Issue AUG). Frontiers Media S.A. https://doi.org/10.3389/fmicb.2014.00465
Lee, S., Park, S., Lee, K., Lee, M., Yu, C., Maeng, J., Kim, H., & Kim, S. (2023). Development of a Simple Direct and Hot-Start PCR Using Escherichia coli-Expressing Taq DNA Polymerase. International Journal of Molecular Sciences, 24(14). https://doi.org/10.3390/ijms241411405
Markoulatos, P., Siafakas, N., & Moncany, M. (2002). Multiplex polymerase chain reaction: A practical approach. Journal of Clinical Laboratory Analysis, 16(1), 47–51. https://doi.org/10.1002/jcla.2058
Promega. (2025) GoTaq® DNA Polymerase. Accesed 28 September of 2025. https://www.promega.com/products/pcr/taq-polymerase/gotaq-dna-polymerase/?catNum=M3001
ThermoFisher. (2025) Platinum™ Taq DNA Polymerase, DNA-free. Invitrogen. Accesed 28 September of 2025. https://www.thermofisher.com/order/catalog/product/15966005.
Torres, L. (2025). Producción, purificación y evaluación catalítica de una Taq ADN polimerasa recombinante.
Tortora, G., Funke, B., & Case, C. (2019). Microbiology: An introduction (13 ed). PEARSON.
Zhra, M., al Saud, A., Alzayer, M., Okdah, L., Tamim, H., Fakhoury, A., & Aljada, A. (2024). Cost-effective in-house COVID-19 reverse transcription-polymerase chain reaction testing with yeast-derived Taq polymerase. Annals of Thoracic Medicine, 19(2), 165–171. https://doi.org/10.4103/atm.atm_180_23
