PCTI 192. LA BIOTECNOLOGÍA INDUSTRIAL Y SUS APLICACIONES EN PROBLEMAS DE LA INDUSTRIA MINERA
Susana Citlaly Gaucin Gutiérrez
Autor de Correspondencia
Dr. Héctor Nolasco Soria
Editor
24/06/2021
Fecha de Aprobación
Biotecnología y Ciencias Agropecuarias
Categoría
Autores
Susana Citlaly Gaucin Gutiérrez1, Hiram Medrano Roldán1, Damián Reyes Jáquez1, David Zazueta Álvarez2
1Instituto Tecnológico de Durango, Felipe Pescador 1830 Ote. Col. Nueva Vizcaya Durango, Dgo. México C.P. 34080, 07040234@itdurango.edu.mx, 2 Universidad Politécnica de Durango.
En la industria minera los compuestos refractarios, constituidos por minerales sulfurados, representan un problema para la extracción de metales como la plata.
Abstract
In the recovery of silver from refractory minerals, conventional processes generate low extraction yields, which is why mineral biotechnology is an effective alternative, where the use of native microorganisms from the mine can extract up to 40% of the encapsulated silver, using as a leaching source the 9K culture medium inoculated with chemolithotrophic microorganisms, from the activity of the microorganisms and the mobility of the ferrous ions in the medium, 67% of the manganese present can be removed.
Keywords: bioleaching, mining industry, low grade recovery, refractory manganese- silver complex
Resumen
En la recuperación de plata, a partir de minerales refractarios, los procesos convencionales generan bajos rendimientos de extracción, por lo cual la biotecnología de minerales es una alternativa eficaz; donde el uso de microorganismos quimiolitotróficos nativos de la mina pueden ayudar en la extracción hasta de un 40% de la plata encapsulada, utilizando como fuente lixiviante el medio de cultivo 9K. Mediante la actividad de estos microorganismos y la movilidad de los iones ferrosos en el medio, puede removerse también el 67% del manganeso presente del mineral.
Palabras clave: biolixiviación, industria minera, recuperación de baja ley, complejos refractarios de manganeso y plata
Problemática
Usuarios
Proyecto
Introducción
La aplicación de procesos biotecnológicos en el tratamiento de minerales de baja ley, para la recuperación de varios metales en solución, se ha practicado durante mucho tiempo (Saavedra y Corton 2014). Recientemente, una variedad de proyectos de investigación se ha dirigido al estudio de la biolixiviación de concentrados de alta ley en condiciones controladas. El fundamento de tales estudios es que este tipo de proceso de lixiviación podría competir con la cianuración. La lixiviación microbiológica está enfocada para plantas más pequeñas, ya que los procesos consumen poca energía y generan un menor impacto ambiental (Medrano-Roldan et al. 2013). Ante los retos que presentan los procesos convencionales, con la presencia de minerales de baja ley o de especies metálicas de interés con baja afinidad a los procesos químicos, la biotecnología de minerales se presenta como una alternativa viable. Esta, actualmente, es una de las principales operaciones de biotecnología aplicada a la industria de la metalurgia extractiva (Morin et al. 2006). La fuente de energía para los microorganismos son el hierro y el azufre, a través de la participación de enzimas (oxidoreductasas), llevando así el intercambio iónico sobre la matriz mineral. Las condiciones elevadas de Fe3+ / Fe2+, en efluentes y lixiviados en minas, son generalmente indicadores de actividad biológica, al igual que la oxidación natural del hierro en los drenajes ácidos (Guerinot 1994). La biolixiviación se puede realizar de diferentes formas, in situ, como la aplicada a minerales de baja ley (Morin et al. 2006). En México, desde la década de los 90s, varios grupos de investigación del Instituto Politécnico Nacional, Universidad Nacional Autónoma de México, Universidad Autónoma de Nuevo León, Instituto Tecnológico de Durango, entre otros, así como algunas empresas mineras, han trabajado en la búsqueda de alternativas para resolver los problemas dentro de esta industria.
Objetivos
Plantear una opción económica y ambientalmente viable en los procesos de extracción para metales encapsulados en complejos refractarios de manganeso.
Materiales y métodos
El proceso de extracción de plata se realizó en un reactor experimental de lixiviación en pilas (heap leching) semi-inundado con medio de cultivo 9K con un volumen de 5L de jales minerales, con altas concentraciones de manganeso, obtenidos de la mina “La Encantada” (Durango, Dgo. Fig. 1). El inóculo bacteriano fue preparado con microorganismos nativos del material de mina, los cuales fueron aislados utilizando el medio de cultivo selectivo 9K modificado (Medrano-Roldan et al. 2013) a un pH inicial de 2, ajustado con ácido sulfúrico 1N. Los cultivos se incubaron por 45 días. La determinación de manganeso y plata se llevó a cabo por espectrometría de absorción atómica (APHA/AWWA/WEF, 2012).

Figura 1. Presa de jales de la mina “La Encantada” (Durango, Dgo.).
Resultados y Discusión
La estrategia biotecnológica utilizada para recuperar minerales de baja ley, mostró que es posible remover hasta un 67% de manganeso en los complejos refractarios como la pirolusita (MnO2); con lo cual, se puede recuperar simultáneamente hasta un 40% de plata. En la Figura 2 se observa que el pH y la concentración de sulfato ferroso tienen un efecto determinante sobre la extracción de manganeso. Métodos reportados (Kane y Cardwell 1974, Acharya et al. 2004) para la remoción de manganeso, con sulfato ferroso (50 g/ L), adición de azúcares y temperatura de 70°C, generan su precipitación en forma de carbonatos. En contraste, un sistema biológico ha mostrado que con la adición de sulfato ferroso, como fuente de energía, las condiciones resultaron adecuadas para que los microorganismos (a un pH inicial cercano a 2) promovieran el intercambio aniónico en la superficie del mineral, de manera que ocurriese la liberación de manganeso a temperatura ambiente (Das et al. 1998). La concentración de sulfato ferroso (Fig.2), probablemente ejerció un efecto favorable sobre la solubilización de manganeso, debido a que los iones ferrosos promueven las reacciones de tipo redox por el ciclo Fe+2/Fe+3 (Juárez 2004). Se pudo observar que en el proceso, a nivel de laboratorio, no tiene efecto significativo la agitación en la remoción de manganeso (Fig.2); lo que determina que un proceso de lixiviación en pilas bajo condiciones inundadas podría funcionar adecuadamente sin agitación a nivel industrial, ya que sería difícil realizar un proceso de mezclado por los costos que esto implica. De esta manera, en un ambiente pobre en oxígeno, algunas bacterias biolixiviantes pueden usar manganeso (IV) como aceptor final de electrones en su cadena respiratoria (Haoran et al. 2005).
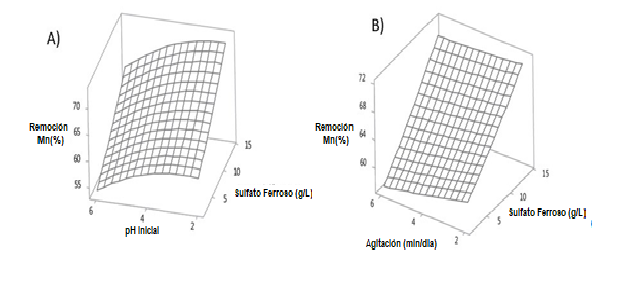
Figura 2. La remoción óptima de manganeso refractario se identifica a un pH 2 (A) y la más alta concentración de FeSO4 y agitación de 2 min/día (B).
La figura 3 muestra los mejores porcentajes de recuperación de plata. Se puede observar que el intervalo de pH óptimo (1.5-2.0) para el crecimiento de los microorganismos afecta negativamente la extracción de plata. Lo anterior, pudiera deberse a que la lixiviación de la fase sólida fue afectada por la alta concentraciones de ácido sulfúrico (utilizado para ajustar el pH) y la acidificación inicial del medio de cultivo, por el ácido generado por el metabolismo de las bacterias. Este efecto se consideró como no deseado, dado que no existe una metodología para la precipitación de plata en la fase líquida por la acción de sustancias ácidas; sin embargo, se ha demostrado que la acción microbiana incluso cuando el manganeso no se ha solubilizado, puede generar porcentajes aceptables en la extracción de plata. Estos resultados muestran que la recuperación de plata de los residuos puede ser posible debido a la remoción de manganeso de la superficie mineral o la posible fractura de la matriz sólida, lo que provoca la producción eficiente de plata por el proceso de cianuración después del tratamiento biológico.
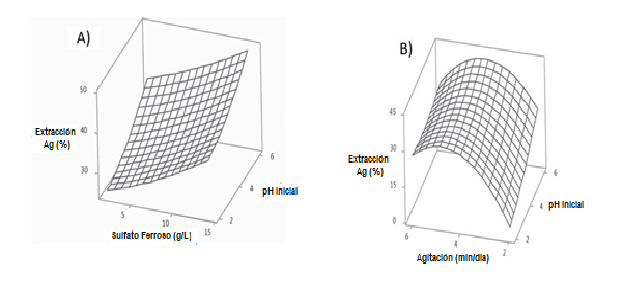
Figura 3. La mayor concentración de plata se identifica a un pH inicial de 6 (C) y la más alta concentración de FeSO4 y agitación de 6 min/día (D).
Conclusiones
En minerales con plata encapsulada en manganeso se ha encontrado que la remoción de manganeso aumenta la concentración de plata recuperada en los procesos de biolixiviación ácida en pilas, con recuperaciones máximas de 50%. Así se ha encontrado que la recuperación de cobre a partir de calcopirita está regida por la transferencia de oxígeno en el sistema, al actuar como aceptor final de electrones. Sin embargo, algunas reacciones regidas por el flujo de iones ferrosos pueden ser promovidas por la acción de microorganismos. La biotecnología de minerales dentro de sus procesos de biolixiviación o biooxidación (in vitro a nivel laboratorio o en pilas a nivel industrial) tiene amplias posibilidades de aplicación en procesos de la industria minera.
Impacto Socioeconómico
Es posible establecer que la evaluación de la economía de ingeniería de los bioprocesos minerales es importante a medida que los nuevos productos pasan de la fase de investigación y desarrollo a la producción comercial y la comercialización. De esta misma manera, se pretende diseñar nuevos procesos para la obtención de materias primas minerales donde el impacto ambiental sea menor.
Referencias
Acharya C, Kar RN, Sukla LB, Misra,VN, (2004). Fungal leaching of manganese ore. Transactions of the Indian Institute of Metals. 57: 501–508
APHA/AWWA/WEF. (2012). Standard Methods for the Examination of Water and Wastewater. Standard Methods, 541.
Das PK, Anand S, Da RP, (1998). Studies on reduction of manganese dioxide by (NH4)2SO3 in ammoniacal medium. Hydrometallurgy. 50: 39–49.
Guerinot M, (1994). Microbial Iron Transport. Annual Review of Microbiology. 48: 743–772.
Haines AK, (1996). Gold 100. Extracting metallurgy of gold. The South African Institute of Mining and Metallurgy. Johannesburg. 2: 227–233.
Haoran L, Yali F, Shouci L, Zhuwei D, (2005). Bioleaching of valuable metals from marine nodules under anaerobic conditions. Minerals Engineering. 18: 1421–1422.
Juárez A. (2004). Biolixiviación de minerales sulfuro-ferroso en jales : de microorganismos involucrados. Universidad de Colima.
Kane WS, Cardwell PH, (1974). “Process for recovering manganese from its ores”, US Patent No. 3:832-165.
Medrano-Roldan H, Galán-Wong LJ, Dávila-Flores RT, (2013). Biotecnología de minerales (1st ed.). México: DGEST.
Morin D, Pinches T, Huismanc J, Friasd C, Norberge A, Forssbergf E, (2006). BioMinE – Integrated project for the development of biotechnology for metal-bearing materials in Europe. Elsevier, Hydrometallurgy, 83(1–4): 69–76.
Saavedra A, Corton E, (2014). Biotecnología microbiana aplicada a la minería. Revista QuímicaViva –, 3: 148–163. https://doi.org/16667948
