PCTI 116. BACTERIAS RESISTENTES A LOS METALES PESADOS DE LAS BATERÍAS ALCALINAS
Mónica M. Galicia-Jiménez
Autor de Correspondencia
Dr. Héctor Nolasco Soria
Editor
04/11/2012
Fecha de Aprobación
Biotecnología y Ciencias Agropecuarias
Categoría
Autores
Adolfo Calderón-Zarza1, Mónica M. Galicia-Jiménez1, Margarita Bernabé Pineda2
1Instituto de Genética. Universidad del Mar. Campus Puerto Escondido, monicagalicia@zicatela.umar.mx
2Instituto de farmacobiología. Universidad de la Cañada.
Los metales potencialmente peligrosos de las baterías incluyen: mercurio, plomo, cobre, zinc, cadmio, manganeso, níquel y litio.
Abstract
We evaluated the minimum inhibitory concentration of heavy metals for 50 strains isolated from sewage sludge, of which only 62% were resistant. With these strains dissolution tests were performed with different concentrations of heavy metals contained in alkaline batteries. By cyclic voltammetry was observed changes from reduced to oxidized states, indicating the interaction of the bacteria with the alkaline batteries components. Also bacterial biofilms structures were observed.
Keywords: bacteria, AA batteries, pollution, heavy metals.
Resumen
Se evaluó la concentración Mínima Inhibitoria de metales pesados para 50 cepas bacterianas aisladas de sedimento de aguas residuales, de las cuales sólo el 62 % fueron resistentes. Con estas cepas se realizaron ensayos de disolución con diferentes concentraciones de los metales pesados contenidos en las pilas alcalinas. Por voltamperometría cíclica se observaron los cambios de estados reducidos a oxidados, indicando la interacción de las bacterias con los componentes de las pilas alcalinas. Así mismo, estructuras bacterianas de biopelículas fueron observadas.
Palabras claves: bacterias, pilas AA, contaminación, metales pesados.
Problemática
Usuarios
Proyecto
Introducción
Desde hace décadas en México, la generación de residuos peligrosos, entre los que se encuentran las pilas, se calcula en 9,000 toneladas diarias, lo cual representa cinco millones de toneladas por año que en su mayoría no tienen un destino final adecuado, debido principalmente al existir industrias insuficientes que se encarguen de su manejo, reciclaje o depósito en lugares adecuados; y también al alto costo que estos procesos implican (Garfias, 1995). Los componentes potencialmente peligrosos de las baterías incluyen: mercurio, plomo, cobre, zinc, cadmio, manganeso, níquel y litio (Gavilán et al., 2009). Además, los orbitales del penúltimo nivel energético de los metales pesados se encuentran completos de electrones y esto les proporciona características y propiedades como la de tener un estado de oxidación distinto al entrar en contacto con el agua, suelo y aire (depende del pH del lugar en que se encuentre), lo cual modifica su reactividad, carga iónica y la capacidad de combinarse con moléculas orgánicas, además tienen una densidad 5 veces mayor a la del agua (Gavilán et al., 2009; Hernández, 2004), por lo que son peligrosos para el ambiente y la salud, causando enfermedades de tipo cardiovascular, de vías respiratorias, cáncer y problemas inmunológicos, entre otras (Prasad, 2008). La capacidad de las bacterias de habitar sitios contaminados por metales pesados, le proporciona un carácter potencial de ser utilizadas en procesos biotecnológicos para disminuir, remediar o incluso para la recuperar de dichos elementos (Cervantes et al., 2006). El propósito de esta investigación es dar los primeros pasos para la búsqueda de compostas de pilas, que ayudados por bacterias resistentes a estos metales eviten mayores daños al ambiente.
Objetivos
El objetivo del proyecto consistió en aislar bacterias nativas en el área urbana de Puerto Escondido, Oaxaca, México para probar su resistencia a los metales pesados de las pilas alcalinas AA y su posterior evaluación en la disolución de los mismos.
Materiales y Métodos
Las cepas bacterianas fueron colectadas, con instrumental y recipientes estériles, del sedimento de la planta de tratamiento de agua residual “El Jícaro”, ubicada en la periferia de Puerto Escondido, Oaxaca, México y trasladados al laboratorio de química de la Universidad del Mar, a una temperatura de 4°C para mantener las cepas viables. Para el aislamiento de las cepas bacterianas se pesó 1 gr de la muestra y se diluyó en 9 ml de agua destilada, y se homogeneizó durante dos minutos. Posteriormente se hicieron diluciones seriadas y fueron inoculadas en agar nutritivo (AN) a 37°C por 24 hrs. Se seleccionaron las unidades formadoras de colonias (UFC) distintas morfológicamente (macro y microscópicamente) y luego se sembraron en tubos con AN para su conservación y en tubos de caldo nutritivo (CN) para su posterior identificación. La identificación de las cepas bacterianas se realizó mediante pruebas bioquímicas convencionales (Bergey, 2000). Para las pruebas de extracción y determinación de los metales pesados (MP) en las pilas alcalinas se separaron y se trituraron hasta obtener un polvo fino que se colocó al interior de una estufa de secado por 24 hrs a 80 ºC (Jaapar, 2002). Posteriormente, se pesaron el contenido de los metales para preparar las disoluciones porcentuales requeridas. Los metales fueron disueltos por medio de una digestión ácida, utilizando agua regia (120 ml de HCl y 100 de HNO3 y calentado a 70°C) (modificado de ISO 11466:1995). Las pruebas de resistencia bacteriana a los MP se realizaron por la técnica de Concentración Mínima Inhibitoria (CMI) por difusión de disco (Bauer et al., 1985) para lo cual se utilizaron discos de papel filtro, los cuales fueron sumergidos en las disoluciones de los MP extraídos de las pilas con las concentraciones 11.8, 22.8, 40 y 140.8 mg/ml-1, utilizando las cepas puras aisladas e incubadas durante 24 hrs a 37 °C. Las cepas resistentes fueron seleccionadas para las pruebas de disolución de los metales de las pilas alcalinas AA. Las pruebas de disolución de metales se realizaron en un matraz Erlenmeyer con 780 ml de CN y 220 ml de la solución de la digestión ácida (modificado de ISO 11466:1995), con concentraciones de 22.8, 40 y 140.8 mg/L de los metales de las pilas alcalinas, a un pH de 5, se le agregó 1 ml de inóculo (de un pool de todas las bacterias que resultaron resistentes en las pruebas de CMI), se incubaron durante 240 hrs a 37 °C en agitación a 120 rpm. Cada 24 h se tomaron dos muestras de 100 ml, una para el análisis microbiológico y la otra muestra se centrifugó a 15,000 rpm a 4oC, 10 min, para el análisis de contenido de MP en la biomasa y el sobrenadante libre de células, ambos se esterilizaron en autoclave (121oC, 15 Lb por 15 min.), se conservaron a 4 °C hasta su análisis en el laboratorio de Ciencias Ambientales del Centro de Investigaciones en Química Sustentable de la Universidad Autónoma del Estado de México. El análisis de disolución de los metales se realizó mediante voltamperometría cíclica ya que esta técnica tiene la posibilidad única de distinguir los diversos estados de oxidación que puede afectar la reactividad y la toxicología de una sustancia (Monroy et al., 2006). Para el análisis de los iones metálicos insolubles (formación de óxidos) presentes en la biomasa se empleó un análisis por medio del espectrofotómetro fotoelectrónico de rayos X (XPS) (Lee, 2002) de la biomasa bacteriana depositada al fondo de los sistemas experimentales, para de esta manera comprobar la presencia de especies insolubles de los metales que son factibles de formarse por la interacción bacteriana (Francis, 2002).
Resultados y Discusión
Como resultado se obtuvieron 50 cepas de las cuales el 62% (31 cepas) de éstas fueron resistentes. Sólo 12 cepas pertenecientes del genero Bacillus estuvieron presentes al final del ensayo de disolución de los metales. La voltamperometría cíclica permitió observar la interacción de las bacterias con los metales en las distintas concentraciones, siendo la más sobresaliente la concentración de 140.8 mg/L (Fig. 1).
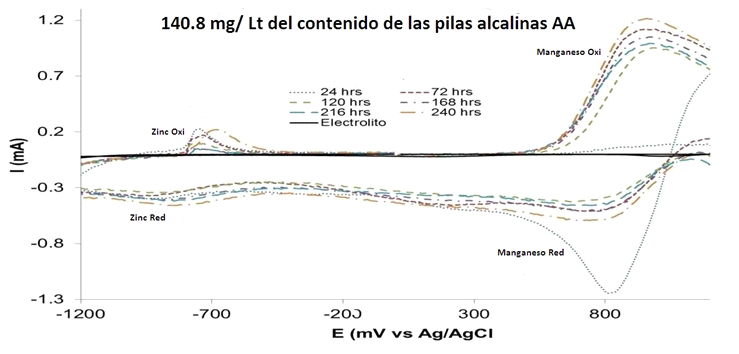
Figura 1. Voltamperograma cíclico correspondiente a la concentración de 140.8 mg/L (140.8 ppm) de los metales pesados contenidos en las pilas alcalinas AA, a una velocidad de escaneo de 100 mV/. Barrido en sentido anódico. En esta figura podemos observar los procesos de oxido-reducción del zinc y manganeso. Las intensidades de los procesos se ven modificadas con respecto al tiempo lo que es un indicativo de que el zinc y del manganeso presentan una interacción por la presencia de las bacterias.
El análisis de la biomasa sedimentada con el XPS nos permitió determinar la presencia de especies insolubles de ambos metales en los sistemas experimentales, formando óxidos en ambos casos y los cuales se precipitan por la interacción con Bacillus (Francis, 2002). Durante el ensayo se observó la formación de biopelículas en los diversos matraces con las diferentes concentraciones de los metales pesados (Fig. 2). Una biopelícula está definida como una colonia de células bacterianas asociadas irreversiblemente o reversiblemente a una superficie, y que está compuesta principalmente por exopolisacáridos (EPS). Los EPS actúan como agentes detoxificantes de metales debido a que tienen alta proporción de grupos funcionales cargados negativamente como grupos carboxilo, fosfato y sulfato, que actúan como sitios de unión a metales (García Meza et al., 2005; Aguilera y col., 2008).
Conclusiones
Se reconoce que los resultados obtenidos no son concluyentes, por lo que abre la posibilidad de proponer más estudios para su aplicación en la remediación de suelos contaminados por metales pesados en México.

Figura 2. Estructuras bacterianas formadas en el ensayo de la disolución de los metales. Se observan estructuras circulares de distinto tamaño y color en los sistemas experimentales con diferentes concentraciones a) 5%, b) 1.25% (concentración de 140.8 mg/L), c) 0.25% de los metales pesados contenidos en las pilas alcalinas AA, conocidos como biopelículas.
Impacto Socioeconómico
Este trabajo es la primera contribución que se realiza para la identificación de bacterias potenciales a ser utilizados para la disminución o eliminación de metales pesados provenientes de las pilas alcalinas.
Referencias
Aguilera A., Souza E.V., Martín U.P.S., Amils R. 2008. Extraction of extracellular polymeric substances from extreme acidic microbial biofilms. Applied Microbiology Biotechnology. 78 (6), 1079-1088.
Bauer, A.W., Kirby, W.M.M., Sherris, J.C. y Turck, M. 1985. Antibiotic susceptibility testing by a standardized single method. American Journal of Pathology.45:493-496.
Cervantes, C., et al. 2006. Interacciones microbianas con metales pesados. Revista Latinoamericana de Microbiología, 48(2):203-210.
García-Meza J.V. 2008. Autotrophic biofilm development on superficial samples on the gold-silver mine tailings, Valenciana (México): Pioneers in tailings remediation?. Bulletin of Environmental Contamination and Toxicology. 80 (1), 53-57.
Gavilán García, A., Rojas Bracho, L., y Barrera Cordero, J. 2009. Las Pilas en México: Un Diagnóstico Ambiental. Instituto Nacional de Ecología. México. 26 p.
Francis, C.A. y Tebo, B.M. 2002. Enzymatic Manganese (II) Oxidation by Metabolically Dormant Spores of Diverse Bacillus Species. Applied and Environmental Microbiology, 874-880 pp
Hernández, H. 2004. Estudio de la capacidad coordinante del diclofenaco sódico {[2-[2,6-Diclorofenil) Amino] Fenilato de sodio} y los iones contaminantes Pb (II),Cd(II), Zn(II) y Mn(II). Tesis de Licenciatura. Quimicofarmacobiología.Departamento de Química y Biología, Escuela de Ciencias, Universidad de las Américas, Puebla.76 p.
ISO (International Organization for Standardization) 11466. (1995) Soil quality – Extraction of trace elements soluble in aqua regia, Genève, Switzerland, 6 pp.
Jaapar, J. y Ahmad, W. A. 2006. Recovery of valuable metals from dry cells batteries. International Conference on Environment. Penang, Malasya, 13-15 p.
Lee, A. Y., Blakeslee, D. M., Powell, C. J., Rumble, J. R. 2002. Development of the web-based NIST X-ray Photoelectron Spectroscopy (XPS) Database. Data Science Journal, 1-12 pp
Monroy M, Cruz R, González I. 2006. Evaluación de la reactividad de sulfuros de hierro y residuos mineros: una metodología basada en la aplicación de la voltamperometría cíclica. Quím. Nova [online]. 29(3):510-519.
Prasad, A. S. 2008. Zinc in Human Health: Effect of Zinc on Immune Cells. En línea. Disponible en: http://www.molmed.org. Consultado el 18 de octubre de 2012.
Vullo, D. L. 2003. Microorganismos y Metales Pesados: Una Interacción en Beneficio del Medio Ambiente. Química Viva, 2(3):93-104.
