PCTI 252-SC-Efectos inmunológicos persistentes de la levadura probiótica Debaryomyces hansenii CBS 8339 en cabritos (Capra hircus) recién nacidos
Carlos Angulo
Autor de Correspondencia
Dr. Héctor Nolasco Soria
Editor
12/12/2025
Fecha de Aprobación
Biotecnología y Ciencias Agropecuarias
Categoría
Autores
Miriam Angulo, Emmanuel Junco y Carlos Angulo
Centro de Investigaciones Biológicas del Noroeste, S.C. (CIBNOR), Grupo de Inmunología y Vacunología, Ave. Instituto Politécnico Nacional 195, Playa Palo de Santa Rita Sur, La Paz B.C.S., 23096, México. eangulo@cibnor.mx
Universidad Autónoma de Baja California Sur (UABCS). Boulevard Forjadores S/N entre Calle Av. Universidad y Calle Félix Agramont Cota Col. Universitario. La Paz, B.C.S., 23080, México.
En los primeros días de vida, los cabritos son muy susceptibles a infecciones porque su sistema inmune (protección contra enfermedades) aún no está completamente desarrollado.
Glosario de términos técnicos
Patógeno: agente biológico que causa una enfermedad (Basset et al., 2003).
Antibiótico: Sustancia utilizada para eliminar o inhibir el crecimiento de bacterias que causan enfermedades (Bentley & Bennett, 2003).
Resistencia antimicrobiana: Capacidad de microorganismos para sobrevivir y multiplicarse a pesar del uso de medicamentos diseñados para eliminarlos (Singh et al., 2018).
Efecto duradero del entrenamiento inmune: Periodo de al menos 30 días en el que persisten la respuesta entrenada del sistema inmune (Torre et al., 2017).
Abstract
Early diseases such as colibacillosis (caused by the pathogen Escherichia coli) affect the survival and growth of goat kids, leading to excessive antibiotic use. This study evaluated whether the beneficial yeast Debaryomyces hansenii can train the defenses of newborn goat kids to improve their response to infections. To test this, the yeast was administered orally (two doses on days 0 and 3), and immunological and metabolic parameters were analyzed at 7 and 30 days after exposure to Escherichia coli. The results show that, one week after training, immune cells increased their defensive activity and adjusted their metabolism to respond more rapidly to the pathogen. Thirty days later, although the metabolic changes (glucose consumption and lactate production) did not persist, the immune functions (phagocytosis, respiratory burst and myeloperoxidase activity) remained enhanced. The above indicates that D. hansenii can improve goat kids’ ability to fight infections.
Keywords: Animal health, beneficial microorganism, defenses.
Resumen:
Las enfermedades tempranas como la colibacilosis (causada por el patógeno Escherichia coli) afectan la supervivencia y el crecimiento de los cabritos y favorecen el uso excesivo de antibióticos. Este estudio evaluó si la levadura benéfica Debaryomyces hansenii puede entrenar las defensas de cabritos recién nacidos para mejorar su respuesta ante infecciones. Para ello, se administró la levadura por vía oral (2 dosis al día 0 y 3) y se analizaron parámetros inmunológicos y metabólicos a los 7 y 30 días, después de la exposición a Escherichia coli. Los resultados muestran que, una semana después del entrenamiento, las células del sistema inmune aumentaron su actividad de defensa y modificaron su metabolismo para responder con mayor rapidez frente al patógeno. Treinta días después, aunque los cambios metabólicos (consumo de glucosa y producción de lactato) no persistieron, las funciones inmunológicas (fagocitosis, la explosión respiratoria y la actividad de la enzima mieloperoxidasa) aumentaron. Esto indica que D. hansenii puede mejorar la capacidad de los cabritos para enfrentar infecciones de forma más eficiente.
Palabras clave: Salud animal, microorganismo benéfico, defensas.
Problemática
Usuarios
Proyecto
Introducción:
En los primeros días de vida, los cabritos son muy susceptibles a infecciones porque su sistema inmune (protección contra enfermedades) aún no está completamente desarrollado. Aunque se usan antibióticos para tratar las enfermedades, su administración inadecuada ha generado microorganismos patógenos resistentes (dañinos para los animales) (Singh et al., 2018). Ante este desafío, se han explorado alternativas naturales que fortalezcan el sistema inmune, como el uso de microorganismos con propiedades probióticas (benéficas). Entre ellos, la levadura Debaryomyces hansenii es capaz de estimular y entrenar el sistema inmune innato (con el que nacen los animales) de animales terrestres y acuáticos (Netea et al., 2016).
Objetivos:
En este trabajo se investigó el efecto de la administración oral de la levadura Debaryomyces hansenii sobre el “entrenamiento” del sistema inmune innato de cabritos recién nacidos a los 7 y 30 días después de la administración.
Materiales y métodos:
El experimento con los animales se realizó de acuerdo con el protocolo aprobado por el comité de ética del Centro de Investigaciones Biológicas del Noroeste, S.C. (CIBNOR-CEI-2024-06). Los animales utilizados en este estudio provinieron de la Unidad Experimental Ovina y Caprina de la Universidad Autónoma de Baja California, Sur.
La cepa D. hansenii CBS 8339 se cultivó en medio YPD (extracto de levadura 5 g/L, peptona 10 g/L y dextrosa 10 g/L; Sigma, St. Louis, MO, USA) a 30 °C, bajo agitación constante de 150 r.p.m. durante 24 h. La biomasa se recuperó por centrifugación (2500 r.p.m., 15 min). La biomasa húmeda (levadura) se administró por vía oral en leche materna de cabra a diez cabritos (5 hembras y 5 machos) de entre 1 y 5 días de edad (grupo Dh). El esquema consistió en dos dosis separadas por tres días (Fig. 1), con una dosis de 5 mg de levadura (biomasa húmeda; 1×109 CFU/mg; Angulo et al., 2019) por kilogramo de peso vivo en cada administración. Otro grupo de diez cabritos recibió únicamente 5 mililitros de leche materna en las mismas condiciones (grupo C). El día 7 se obtuvo una muestra sanguínea para el aislamiento de monocitos, que son células del sistema inmune innato (Murray, 2018). Las células (1 × 10⁶ monocitos/mL) se expusieron a la bacteria patógena Escherichia coli (1 × 10⁸ UFC/mL) y se mantuvieron en incubación durante 24 h para posteriormente analizar parámetros inmunológicos y metabólicos.
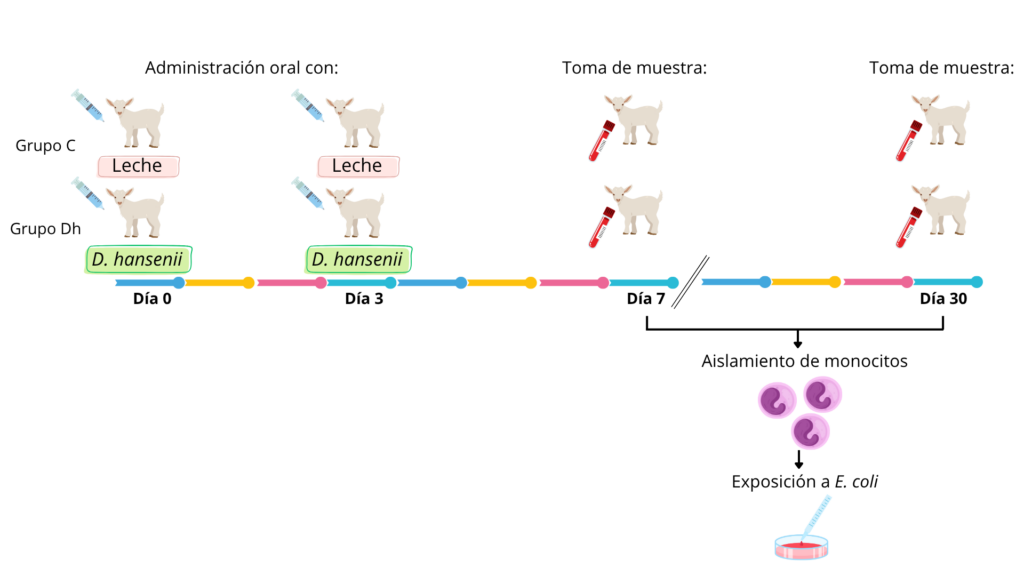
Figura 1. Esquema de administración de D. hansenii en cabritos recién nacidos; así como de la toma de muestras y de la exposición a E. coli.
Además, los cabritos permanecieron en sus corrales y fueron monitoreados para garantizar su bienestar durante 30 días. Después de este periodo, se repitieron los mismos análisis al final del periodo para evaluar si el efecto del entrenamiento inmune persistía. El entrenamiento inmune es un proceso que consiste en “enseñar” a las células de defensa a reaccionar mejor ante un patógeno (Netea et al., 2016) y se ha considerado un efecto de entrenamiento duradero desde los 30 días (Torre et al., 2017).
Los parámetros inmunológicos evaluados en los monocitos de los cabritos fueron: la actividad fagocítica (Sanchez et al. 2021), la actividad de la explosión respiratoria (Kemenade et al., 1994), la producción de óxido nítrico (Neumann et al., 1995), la actividad de la mieloperoxidasa (Quade y Roth, 1997). También se midieron parámetros metabólicos como consumo de glucosa (Díaz et al., 2020) y producción de lactato (Zhang et al., 2017).
Los datos se analizaron con un software estadístico especializado. Cada prueba se realizó por triplicado y los resultados se expresaron como promedios. Para identificar diferencias entre grupos, se aplicaron análisis de varianza (ANOVA) y comparaciones estadísticas posteriores (prueba de Duncan; p < 0.05).
Resultados y discusión:
Durante la inmunidad entrenada, las células del sistema inmune mejoran algunas funciones y ajustan su metabolismo, lo que las prepara para responder de manera más eficiente ante una infección (Fanucchi et al., 2021). Por ejemplo, la fagocitosis es una actividad (mecanismo) fundamental en la que los monocitos reconocen, atrapan y destruyen a los patógenos. Para eliminarlos, estas células producen compuestos tóxicos para los patógenos, como el óxido nítrico y las especies (reactivas) de oxígeno; además de activar enzimas como la mieloperoxidasa, que generan otros compuestos que destruyen patógenos invasores (Bekkering et al., 2016; Arneth, 2021). Por otro lado, durante el entrenamiento inmune, las células pueden ajustar su metabolismo para obtener la energía que necesitan (Stienstra et al., 2017). Cuando se activan, requieren un acceso rápido a fuentes de energía para llevar a cabo los procesos de la respuesta inmune. Un ejemplo es la glucólisis, un camino dentro de las células que les permite obtener energía de la glucosa que consumimos (Ferreira et al., 2024). En este estudio se observó que 7 días después del entrenamiento inmune con el probiótico y tras la infección con E. coli, los monocitos de los cabritos aumentaron parámetros inmunológicos como la fagocitosis y la producción de óxido nítrico, y metabólicos como el consumo de glucosa y la producción de lactato (es el producto final de la glucólisis que indica que las células están aprovechando la glucosa). Estos resultados sugieren que el sistema inmune innato no solo activó sus mecanismos de protección, sino que también ajustó su metabolismo para obtener la energía necesaria y responder de manera más rápida y eficaz frente al patógeno. Treinta días después del entrenamiento, algunos parámetros inmunológicos aumentaron, como la fagocitosis, la explosión respiratoria y la actividad de la enzima mieloperoxidasa (Fig. 2), pero no el consumo de energía y la producción de lactato. Esto sugiere que los ajustes metabólicos de las células en el entrenamiento inmune por el probiótico D. hansenii podría ser un evento temporal que impulsa la respuesta inmune inicial (Mitroulis et al., 2018); pero, interesantemente, las funciones del sistema inmune innato pueden mantenerse por más tiempo, permitiendo una respuesta reforzada (Théroude et al., 2021) incluso después de semanas.
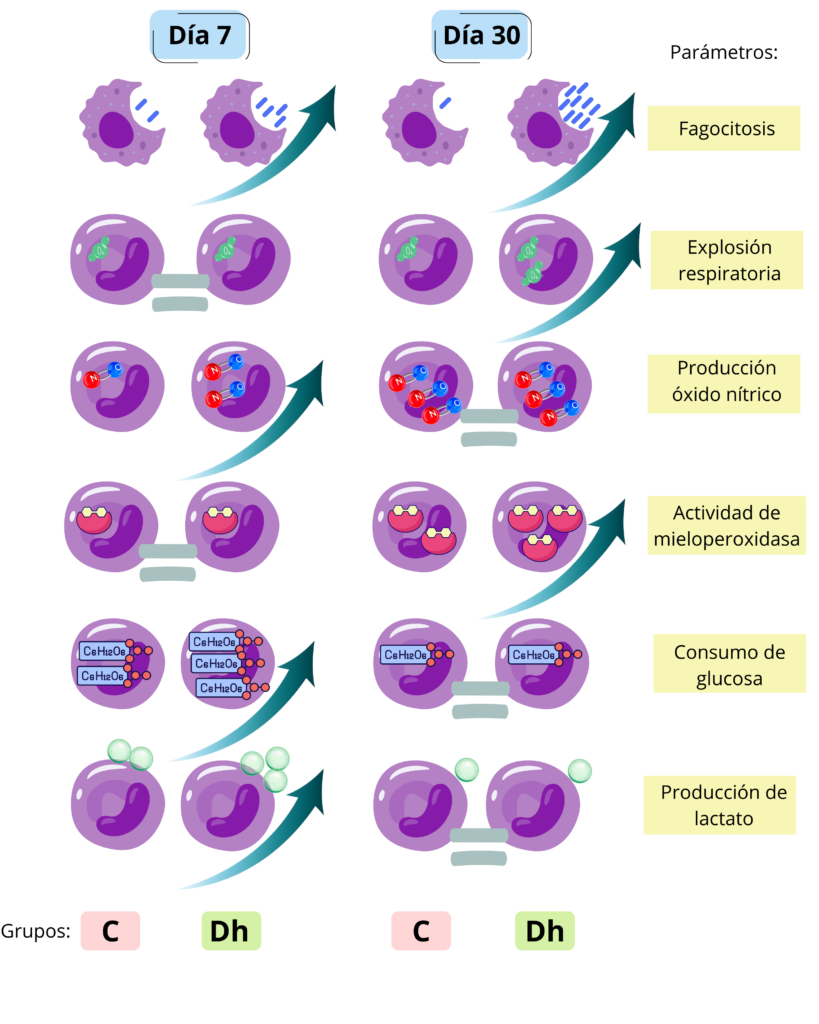
Figura 2. Respuesta de los parámetros inmunológicos (viabilidad, fagocitosis, explosión respiratoria, producción óxido nítrico y actividad mieloperoxidasa) y metabólicos (consumo de glucosa y producción de lactato) en monocitos de cabritos del grupo control (C) y del grupo que recibió D. hansenii (Dh) después de la infección con E. coli. La flecha dirigida hacia arriba indica que el parámetro aumentó gracias a la administración de D. hansenii, indicando un fortalecimiento de la respuesta inmune en la capacidad de las células para responder a infecciones. El signo igual (=) señala que ese parámetro no mostró cambios con la administración de D. hansenii.
Conclusiones:
La levadura probiótica Debaryomyces hansenii entrenó las defensas inmunes de los cabritos recién nacidos, fortaleciendo parámetros clave, mejorando con ello su capacidad de responder a infecciones. Aunque los cambios metabólicos no se mantuvieron a largo plazo, las funciones inmunes mejoradas persistieron incluso 30 días después, indicando un efecto duradero sobre la inmunidad innata.
Impacto Socioeconómico
El entrenamiento del sistema inmune innato de los cabritos con D. hansenii podría reducir las enfermedades en las primeras semanas de vida, disminuyendo pérdidas por mortalidad y bajo crecimiento. Además, al funcionar como una alternativa natural al uso excesivo de antibióticos, ayudaría a reducir costos en tratamientos veterinarios y a frenar la resistencia antimicrobiana, un problema que afecta la salud animal, humana y ambiental.
Referencias
Angulo, M., Reyes-Becerril, M., Cepeda-Palacios, R., Tovar-Ramírez, D., Esteban, M. Á., & Angulo, C. (2019). Probiotic effects of marine Debaryomyces hansenii CBS 8339 on innate immune and antioxidant parameters in newborn goats. Applied microbiology and biotechnology, 103(5), 2339-2352.
Arneth, B., 2021. Trained innate immunity. Immunol. Res. 69 (1), 1–7.
Basset, C., Holton, J., O’Mahony, R., & Roitt, I. (2003). Innate immunity and pathogen–host interaction. Vaccine, 21, S12-S23.
Bekkering, S., Blok, B. A., Joosten, L. A., Riksen, N. P., van Crevel, R., & Netea, M. G. (2016). In vitro experimental model of trained innate immunity in human primary monocytes. Clinical and Vaccine Immunology, 23(12), 926-933.
Bentley, R., & Bennett, J. W. (2003). What is an antibiotic? Revisited. Advances in applied microbiology, 52, 303-332.
Diaz, P. A. R., Camargo, D. E. G., Ondo-Méndez, A., & Gómez-Alegría, C. J. (2020). A colorimetric bioassay for quantitation of both basal and insulin-induced glucose consumption in 3T3-L1 adipose cells. Heliyon, 6(2).
Fanucchi, S., Domínguez-Andrés, J., Joosten, L. A., Netea, M. G., & Mhlanga, M. M. (2021). The intersection of epigenetics and metabolism in trained immunity. Immunity, 54(1), 32-43.
Ferreira, A. V., Domínguez-Andrés, J., Merlo Pich, L. M., Joosten, L. A., & Netea, M. G. (2024, August). Metabolic regulation in the induction of trained immunity. In Seminars in Immunopathology (Vol. 46, No. 3, p. 7). Berlin/Heidelberg: Springer Berlin Heidelberg.
Kemenade, B. L. V. V., Groeneveld, A., Rens, B. T. V., & Rombout, J. H. (1994). Characterization of macrophages and neutrophilic granulocytes from the pronephros of carp (Cyprinus carpio). Journal of experimental biology, 187(1), 143-158.
Mitroulis, I., Ruppova, K., Wang, B., Chen, L. S., Grzybek, M., Grinenko, T., & Chavakis, T. (2018). Modulation of myelopoiesis progenitors is an integral component of trained immunity. Cell, 172(1), 147-161.
Murray, P. J. (2018, February). Immune regulation by monocytes. In Seminars in immunology (Vol. 35, pp. 12-18). Academic Press.
Netea, M. G., Joosten, L. A., Latz, E., Mills, K. H., Natoli, G., Stunnenberg, H. G., & Xavier, R. J. (2016). Trained immunity: a program of innate immune memory in health and disease. Science, 352(6284), aaf1098.
Neumann, N. F., Fagan, D., & Belosevic, M. (1995). Macrophage activating factor (s) secreted by mitogen stimulated goldfish kidney leukocytes synergize with bacterial lipopolysaccharide to induce nitric oxide production in teleost macrophages. Developmental & Comparative Immunology, 19(6), 473-482.
Singh, D. D., Pawaiya, R. V. S., Gururaj, K., Gangwar, N. K., Mishra, A. K., Singh, R., & Kumar, A. (2018). Detection of Clostridium perfringens toxinotypes, enteropathogenic E. coli, Rota and corona viruses in the intestine of neonatal goat kids by molecular techniques. Indian J Anim Res, 88(6), 655-661.
Quade, M. J., & Roth, J. A. (1997). A rapid, direct assay to measure degranulation of bovine neutrophil primary granules. Veterinary immunology and immunopathology, 58(3-4), 239-248.
Sanchez, V., Rosales-Mendoza, S., Monreal-Escalante, E., Murillo-Álvarez, J. I., & Angulo, C. (2021). Conjugation of β-glucans on heat-stable enterotoxin (ST) to enhance the immunogenic response in mouse leucocytes. Materials Science and Engineering: C, 118, 111464.
Stienstra, R., Netea-Maier, R. T., Riksen, N. P., Joosten, L. A., & Netea, M. G. (2017). Specific and complex reprogramming of cellular metabolism in myeloid cells during innate immune responses. Cell metabolism, 26(1), 142-156.
Torre, C., Abnave, P., Tsoumtsa, L. L., Mottola, G., Lepolard, C., Trouplin, V., & Ghigo, E. (2017). Staphylococcus aureus promotes Smed-PGRP-2/Smed-setd8-1 methyltransferase signalling in planarian neoblasts to sensitize anti-bacterial gene responses during re-infection. EBioMedicine, 20, 150-160.
Zhang, W., Guo, C., Jiang, K., Ying, M., & Hu, X. (2017). Quantification of lactate from various metabolic pathways and quantification issues of lactate isotopologues and isotopmers. Scientific reports, 7(1), 8489.PCTI 252-Levadura probiotica-cabritos
